Boussonniere, Anne

Boussonniere, Anne

Parcours
Depuis Septembre 2012 : Maître de conférences
Laboratoire IMMM, Université du Maine (Le Mans)
Décembre 2010-Aout 2012 : Post-doctorat
Chemistry Department, University of Pittsburgh (PA, USA)
Pr. Dennis P. Curran
« Étude de la réactivité des complexes N-Heterocyclic Carbene-boranes »
Octobre 2007-Novembre 2010 : Thèse
Laboratoire CEISAM, Université de Nantes
Pr. Jacques Lebreton, Dr. Fabrice Dénès
« Utilisation des acétals d’aluminium α-halogénés en chimie radicalaire »
Activités de recherche
Réactions de carbolithiation asymétriques
Membres intervenants : Anne Boussonnière, Anne-Sophie Castanet

Une nouvelle classe de ligands 1,2-aminoéther chiraux, facilement accessibles à partir d'acides α-amino- ou α-hydroxy naturels, s'est avérée particulièrement efficace en termes de conversion et de stéréocontrôle (jusqu'à 95: 5 er) en réaction de carbolithiation intramoléculaire. Ces derniers surpassent généralement le ligand de référence : la spartéine. De plus, ce nouveau type de ligand peut être utilisé en une quantité sous-stoechiométrique (0,25 équiv) sans perte significative d'énantiosélectivité.
Guyon, H.; Boussonnière, A.; Castanet, A.-S., Readily Accessible 1,2-Amino Ether Ligands for Enantioselective Intramolecular Carbolithiation. J. Org. Chem 2017, 82, 4949-4957. http://dx.doi.org/10.1021/acs.joc.7b00423
Synthèse de d’acides benzoïques fonctionnalisés par SNAr
Membres intervenants : Anne Boussonnière, Anne-Sophie Castanet, Jacques Mortier
Nous avons récemment développé la réaction de Substitution Nucléophile Aromatique sur les Acides Benzoïques non-protégés (SNArAB). Ce procédé efficace consiste à soumettre différents acides ortho-fluorés ou méthoxylés à l’action de nucléophiles de type alkyl ou 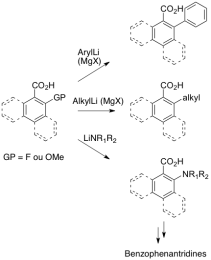 aryllithiens ou Grignard mais aussi avec les amidures de lithium. Cette approche constitue une alternative intéressante pour la construction de noyaux aromatiques fonctionnalisés souvent préparés par couplage catalysé par les métaux de transition, sans étape de protection/ déprotection de la fonction acide. Les dérivés d’acides anthraniliques, obtenus avec les amidures de lithium, sont aujourd’hui valorisés par le développement de la synthèse de benzophénantridines à partir de ces précurseurs.
aryllithiens ou Grignard mais aussi avec les amidures de lithium. Cette approche constitue une alternative intéressante pour la construction de noyaux aromatiques fonctionnalisés souvent préparés par couplage catalysé par les métaux de transition, sans étape de protection/ déprotection de la fonction acide. Les dérivés d’acides anthraniliques, obtenus avec les amidures de lithium, sont aujourd’hui valorisés par le développement de la synthèse de benzophénantridines à partir de ces précurseurs.
Chapitre de livre :Asymmetric Nucleophilic Aromatic Substitution by A.-S. Castanet, A. Boussonnière and J. Mortier*, Chapter 8, in Arene Chemistry: Reaction Mechanisms and Methods for Aromatic Compounds , edited by J. Mortier, John Wiley & Sons, Inc., Hoboken NJ, USA (2016) in press
R. Aissaoui, A. Nourry, A. Coquel, T. T. H. Dao, A. Derdour, J.-J. Helesbeux, O. Duval, A.-S. Castanet, J. Mortier J. Org. Chem. 2012, 77, 718.
J. Mortier, A.-S. Castanet, A. Nourry, M. Belaud-Rotureau FR Patent FR2961204 (2011), WO Patent WO2011101604A1 (2011).
J. Mortier, A.-S. Castanet, M. Belaud-Rotureau FR Patent FR2956662A1 (2011), WO Patent WO2011101599A1 (2011).
M. Belaud-Rotureau, T. T. Le, T. H. T. Phan, T. H. Nguyen, R. Aissaoui, F. Gohier, A. Derdour, A.-S. Castanet, K. P. P. Nguyen, J. Mortier Org. Lett. 2010, 12, 2406.
Fonctionnalisation de noyaux aromatiques par métallation par les composés organométalliques polaires
Membres intervenants : Anne Boussonnière, Anne-Sophie Castanet, Jacques Mortier
Nous nous intéressons à la fonctionnalisation sélective de noyaux aromatiques par métallation dirigée à l’aide de composés organométalliques polaires. Nos travaux portent notamment sur l’évaluation de nouveaux groupements ortho-directeurs, tels que la fonction acide carboxylique ou le substituant phenyldiazenyle. La compréhension des mécanismes réactionnels est au cœur de nos préoccupations et nous avons pour la première fois étudié et rationalisé les mécanismes des réactions de métallation à distance (Directed remote Metalation DreM).

Chapitre de livre : Directed Metalation of Arenes with Organolithiums, Lithium Amides, and Superbases by F. R. Leroux* and J. Mortier*, Chapter 26, in Arene Chemistry: Reaction Mechanisms and Methods for Aromatic Compounds , edited by J. Mortier, John Wiley & Sons, Inc., Hoboken NJ, USA (2016) in press
Nguyen, T. T. T.; Boussonnière, A.; Banaszak, E.; Castanet, A.-S.; Nguyen, K. P. P.; Mortier, J., J. Org. Chem. 2014, 79 (6), 2775-2780.
D. Tilly, J. Magolan, J. Mortier, Chem. Eur. J. 2012, 18, 3804.
N. H. Nguyen, C. Len, A.-S. Castanet, J. Mortier Beilstein J. Org. Chem. 2011, 7, 1228.
D. Tilly, J.-m. Fu, B.-p. Zhao, M. Alessi, A.-S. Castanet, V. Snieckus, J. Mortier Org. Lett. 2010, 12, 68.
Activités d'enseignement
Enseignement de la Chimie Organique et de la Chimie Analytique, DUT et Licence Professionnelle de Chimie.
Etablissement : IUT de Chimie du Mans